阿爾茲海默病走出“技術沉沒周期”
本文系基于公開資料撰寫,僅作為信息交流之用,不構成任何投資建議。
1906年,美國發明家德·福雷斯特發明了電子三極管,奠定了現代電子學的基石。然而,在人類攻破突破電子學瓶頸后,卻在醫藥領域遇到了新的“瓶頸”。
在同年11月舉行的第37屆精神病學家會議上,一位名叫阿洛伊斯·阿爾茨海默的醫生,向世界報告了一種全新的精神疾病。在對一例具有進行性癡呆表現的51歲女性遺體進行解剖后,他驚人的發現患者腦內遍布著大量深色淀粉樣斑塊。四年后,這種疾病被命名為阿爾茨海默病(簡稱AD)。
此后100多年的時間中,無數學者、藥企在阿爾茨海默病藥物研發中投入大量的時間與金錢,然而換來的卻只有一個又一個的失敗案例。
根據美國藥物生產與研發協會發布的研究報告,僅2000-2017年間,全球累計在阿爾茨海默病藥物上的研發投入就超過6000億美元,失敗的臨床藥物超過300種,失敗率高達99.6%,占所有藥物研發失敗率首位。
攻克阿爾茨海默病,不僅擁有極大的財富價值,甚至已經成為當今世界醫藥人迫切想要實現的夢想之一。
01
AD陷入“技術沉沒周期”
人們對于AD的探索,猶如盲人摸象,一直沒有找到準確的方向。
認知下降,是AD的典型特征,但它同時也是自然衰老的特征之一,兩者之間的最大區別在于AD會加速認知下降的速度。即使如此,但這種認知下降也是一種極為漫長的過程,很可能長達二十年時間,如此長的時間跨度造成了人類攻克AD的道路舉步維艱。

圖:衰老與阿爾茲海默病,來源:西部證券
盡管人類已經與AD奮戰百年,但卻始終沒有準確找到它的發病機制,一切仍舊是個謎團。為了接近真相,科學家提出了多種假說來進行驗證,如Aβ級聯假說、Tau蛋白異常磷酸化假說、膽堿能假說。
但可惜的是,至今為止并沒有哪一種假說得到了業界的公認,這才是為何人類在AD領域毫無收獲的本質原因。
◆Aβ級聯假說
淀粉樣斑塊是AD的主要病理特征之一,它是由Aβ沉積形成,自然也就被認為是人類攻破AD的突破口之一。Aβ級聯假說成為目前最主流的AD藥物研發路徑。
這種假說認為,在正常生理條件下,Aβ的生成與清除處于一個動態平衡的過程,但在病理情況下,Aβ生成增多或者清除減少,導致平衡被打破。Aβ過度沉積在腦內從而引起了一系列的病理過程,這些病理過程反過來又使Aβ增多,形成了級聯式的放大效應。

圖:Aβ級聯假說示意圖
基于此,有科學家提出選擇性結合和消除Aβ淀粉樣蛋白聚集體的方式,以此來尋求扭轉AD中的神經退行性過程。
◆Tau蛋白異常磷酸化假說
AD患者的病理特征并非只有淀粉樣斑塊,神經元纖維纏結也是主要病理特征之一,它是由神經原纖維異常聚集而形成的,其主要成分是高度磷酸化的Tau蛋白。

圖:Tau蛋白過度磷酸化假說示意圖,來源:中國銀河證券
當Tau蛋白發生高度磷酸化時,可以從微管中解離出來,失去對微管的穩定作用,導致物質運輸受損、神經纖維退化,從而引起AD癥狀。
◆膽堿能假說
膽堿能假說是最早的一種關于AD致病機理的學說。
乙酰膽堿與人的認知和記憶密切相關,而AD患者腦內的膽堿能神經元出現嚴重缺失的情況,中樞膽堿能神經遞質不足,從而導致定向力障礙、記憶減退、行為和個性改變等。
目前已經上市的AD藥物,大多數根據膽堿能假說研發的,但顯然它們并沒有完全解決人類在AD上的問題。
致病因素成謎、病程進展周期長、臨床指標差異大、診斷難度大,AD新藥研發陷入長時間的“技術沉沒周期”。
02
藥企“研發黑洞”
回溯藥企AD研發歷程,堪稱一部人類藥物研發失敗史。
2012年,強生/輝瑞的單抗藥物Bapineuzumab的III期臨床試驗失敗;
2014年,羅氏宣告Gantenerumab的III期臨床試驗失敗;
2016年,禮來宣告III期臨床藥物Solanezumab沒有達到主要臨床終點;
2017年,默沙東宣布停止開發BACE抑制劑藥物Verubecestat;
2018年,強生宣布其終止了BACE抑制劑劑Atabecestat II/III期臨床試驗……
無數藥企投入巨額資金卻都折戟沉沙,不能不讓人生出絕望的挫敗感。
在2021年之前,FDA僅批準過6種治療AD的藥物,包括:他克林(Tacrine)、多奈哌齊(Donepezil)、卡巴拉汀(Revastigmine)、加蘭他敏(Galantamine)、美金剛(Menantine)以及美金剛/多奈哌齊復方制劑。

圖:獲批上市的部分AD藥物,來源:天風證券
其中,前四種都是基于膽堿能假說而開發的乙酰膽堿酶(AchE)抑制劑;美金剛為N-甲基-D-天冬氨酸(NMDA)受體拮抗劑,但這些藥物都只能改善患者的癥狀,不能減輕AD的病理變化,也不能逆轉或減緩疾病進程。
同時,目前已獲批的AchE抑制劑都有不同程度的副作用。1993年獲批的他克林,會損傷線粒體,抑制DNA合成蛋白質,誘導細胞凋亡,導致嚴重的不良反應,臨床表現主要是肝毒性和胃腸道反應,最終無奈退市;多奈哌齊是我國使用最多的AD藥物,其嚴重不良反應表現包括神經紊亂(如躁狂癥、攻擊性行為和暴力行為等)。
2019年,綠谷制藥的甘露特鈉膠囊在國內獲批上市,用于治療輕度至中度AD,改善患者的認知功能,是我國第一款治療AD的原創新藥。其作用機制是重塑腸道菌群,抑制腸道細菌氨基酸型神經炎癥,從而抑制AD。
然而,該藥自上市以來就一直爭議不斷,主要疑問指向其Ⅲ期臨床試驗周期過短、效果評估依據不充分、藥物作用機理闡釋不明、療效曲線突變詭異等方面。因此,即使進入醫保后價格大幅下降,銷售額也遠沒有想象中的理想。
隨著全球人口老齡化的加劇,AD患者數量持續升高,據World Alzheimer Report數據顯示,2015年AD患者人數為4680萬,預計2030年增長至7470萬,到2050年時,這個數字將會達到1.3億。
“無藥可治”的困境讓AD成為全球暗藏機遇最大的藥物品類,也有望成為繼心血管疾病、腦血管疾病和癌癥之后,全球第四大藥物市場。
03
百煉終成鋼
傳統療法遲遲無法滿足AD用藥需求的情況下,人類終于在2021年取得了新的突破。
2021年6月,FDA批準渤健的Aduhelm上市,這是第一款基于Aβ級聯假說的藥物,也是第一款治療AD本身的藥物。Aduhelm選擇性識別Aβ構象表位的免疫球蛋白G1(IgG1)單克隆抗體,與患者腦組織中的Aβ沉積結合,激活免疫系統,清除大腦中的沉積蛋白,從而影響AD發病進程。
基于臨床數據,渤健向世人證明,Aduhelm可以顯著使患者的淀粉樣斑塊減少,這也是它之所以能夠獲得FDA批準的原因。但這種淀粉斑塊到底是不是阿爾茲海默癥的誘發因素,依然存在爭議,而Aduhelm并未向市場證明這一點,同時Aduhelm還存在明顯的副作用,這也是它最終商業化失敗的原因。
不過,Aduhelm的失敗并沒有讓渤健放棄AD藥物研發,基于Aduhelm的失敗經驗,渤健在兩年之后帶著另一款產品Leqembi重新回到大眾視野,讓人們再次看到了攻克AD的曙光。
2023年1月,FDA宣布完全批準由衛材和渤健聯合開發的AD新藥侖卡奈單抗(Leqembi),用于治療早期AD患者的上市,成為全球首個能延緩AD進程的藥物。2024年1月,該藥在中國獲批。
III期臨床研究結果表明,與安慰劑相比,Leqembi治療組患者CDR-SB(量化癡呆癥狀的各種嚴重程度)下降減少了27%。在意向治療(ITT)人群的分析中評分差異值為-0.451(p=0.00005)。在安全性方面,Leqembi顯著降低了腦腫脹的發生率,接受Leqembi治療的患者中僅有13%出現腦腫脹。由于其良好的安全性數據,上市后未被添加“黑框警告”。

圖:Leqembi達到了臨床主要終點,來源:衛材公告
Leqembi的成功獲批初步驗證了Aβ假說的有效性,是AD領域藥物開發的標志性事件,被認為是AD治療的新開端。
在Leqembi上市的半年之后,禮來也實現了AD領域的突破,披露了AD新藥Donanemab的最新完整3期臨床數據。與安慰劑相比,接受Donanemab治療的受試者進展到疾病下一階段的風險降低了39%;52%的受試者在1年內達到了淀粉樣蛋白斑塊清除的要求,72% 的受試者在18個月內完成。
從臨床研究數據來看,Donanemab的療效更優于Leqembi,禮來也就此提交了上市申請。不過,這并沒有幫助Donanemab順利上市,FDA在今年3月份最終決定推遲Donanemab藥物的上市批準,并將組織外部專家會議討論該藥物的安全性和有效性。
04
AD研發終現曙光
Leqembi的成功,打開了AD治療領域新世界的大門,已然成為AD藥物研發新路徑。
接下來,各大藥企或將沿著這一路徑開始進行療效和安全性的比拼。
除了Leqembi和Donanemab之外,在AD治療領域,有127種潛在藥物正在進行共164項臨床試驗。其中,處于III期臨床階段的試驗共48項,涵蓋32款藥物;處于II期臨床階段的試驗共90項,涵蓋81款藥物;處于I期臨床階段的試驗共26項,涵蓋25款藥物。
基于Aβ假說的療法是其中資金和研究投入最多的類型,進入臨床開發的產品還有禮來的Remternetug、Annovis Bio的buntanetap、勃林格殷格翰的iclepertin、阿斯利康/ Cerveau Technologies等。
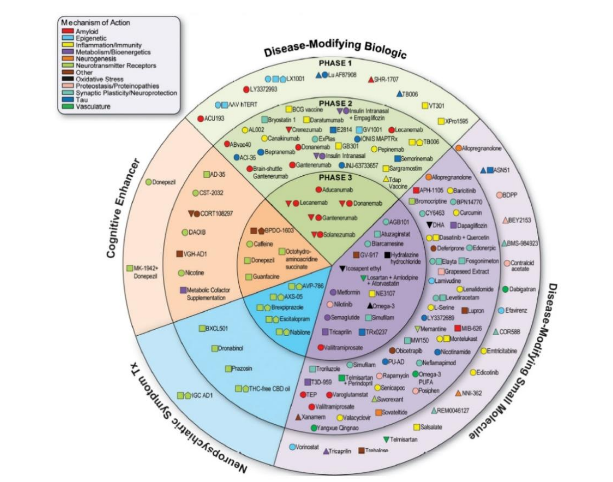
圖:AD在研藥物進展情況
除靶向Aβ路徑外,還有其他很多研發路線也在不斷取得進展,包括在糖尿病和減肥領域大放異彩的GLP-1藥物司美格魯肽,針對AD適應癥的開發正處于III期臨床階段。
對于AD而言,越早發現,越早治療,就越容易延緩病程。然而,目前尚沒有針對AD的早篩產品上市。
基于這一背景,不少藥企選擇跳過早期診斷環節,直接研發AD疫苗,希望通過自身免疫的方式清除Aβ淀粉樣蛋白或Tau 蛋白,為治療阿爾茨海默病開辟了另一條道路。這其中,AC Immune和強生共同研發的AD的疫苗ACI-24.060于2023年6月獲得FDA授予的突破性療法資格認定,目前正在進行II期臨床試驗。
AD領域又燃起星星之火,有望點燃AD賽道長期被抑制的火焰,隨著越來越多的資本入局,人類或將開始在AD賽道全力奔跑。
原文標題 : 阿爾茲海默病走出“技術沉沒周期”

請輸入評論內容...
請輸入評論/評論長度6~500個字
圖片新聞
最新活動更多
-
即日-10.29點擊報名>> 【免費參會】2025韓國智能制造及機械設備企業貿易洽談會
-
即日-12.12點擊報名>>> 【免費試用】宏集運輸沖擊記錄儀
-
即日-12.31立即下載>> 【限時下載】《2025激光行業應用創新發展藍皮書》
-
精彩回顧立即查看>> 高價值貨物的‘數字保鏢’:沖擊記錄儀重塑貨運安全與效率
-
精彩回顧立即查看>> 【在線研討會】解析安森美(onsemi)高精度與超低功耗CGM系統解決方案
-
精彩回顧立即查看>> 【在線會議】CAE優化設計:醫療器械設計的應用案例與方案解析
-
5 創新藥泡沫破了?
-
10 抗體可變區多樣性的來源







 分享
分享












